話題|認知症の薬

全国紙で認知症の特集があり、次のような記事が掲載されました。
-2022年6月24日記事-
認知症の不明届け出、最多 昨年1万7636人、9年連続増 警察庁
9年連続で前年を上回り、統計を取り始めた2012年以降で過去最多だったことがわかった。警察庁が23日発表した。昨年より前に行方不明になった人も含め、昨年中に遺体で見つかった人は450人だった。
-2022年7月1日記事-
高齢者6人に1人 602万人、65歳以上の認知症
65歳以上で認知症の人は約602万人――。政府が2020年時点について推計した数字だ。高齢者の約6人に1人が認知症という計算になる。
研究では18年時点の国民健康保険や介護保険などのデータを使った。認知症のなかで最も多いアルツハイマー型の患者数は、65歳以上の人口のおよそ1割にあたる約360万人と推計。
アルツハイマー型認知症の治療薬
そこで気になるのが認知症の薬、特にアルツハイマー型認知症に対する治療薬です。
少し前に認知症薬に関する次のようなニュースがありました。
“日本の製薬会社エーザイ(以下エーザイ)が厚生労働省に申請していた新しいアルツハイマー型認知症治療薬:一般名アデュカヌマブが、2021年12月に承認見送り、継続審議となった。”
この記事にある”アデュカヌマブ“とはどんな薬なのでしょうか?
1.アデュカヌマブ開発と製品化への経緯
ニュースにある、承認ならなかったアルツハイマー型認知症治療薬”アデュカヌマブ”とはどのようなものか、その経緯を見てみると
20??年 米製薬会社バイオジェン(以下バイオジェン)がアルツハイマー型認知症(以下AD)の新薬アデュカヌマブの開発開始
2014年8月 バイオジェンがアデュカヌマブの臨床試験開始
同年、ベルギーの製薬会社ヤンセンと米製薬会社ファイザーが開発していたAD薬と、米製薬会社イーライリリーが開発していたAD薬はいずれも臨床試験で有効な結果が出ず、開発中止となっている。
2017年10月 エーザイがバイオジェンと手を組み、アデュカヌマブを共同で開発、製品化を目指すことになる。
2020年7月 バイオジェンが米FDA(食品医薬品局)にアデュカヌマブをAD薬としての承認申請
2020年12月 エーザイがアデュカヌマブをAD薬として日本の厚労省へ承認申請
2021年6月 FDAはアデュカヌマブを条件付き(追加の臨床試験を求める)で承認
2021年12月 厚労省はアデュカヌマブの承認見送り決定、継続審議となる
2022年3月 エーザイはバイオジェンとの共同開発・製品化から手を引くと発表
2022年4月 米保健当局は、アデュカヌマブを高齢者向けの公的保険の適応としないと発表
2022年4月 バイオジェンは欧州医薬品庁に承認申請していたアデュカヌマブの申請を取り下げる
2.ADの病理について
ADの原因は、アミロイドβと言われる脳内の老人斑とタウ蛋白といわれる神経原線維の変化と言われています。
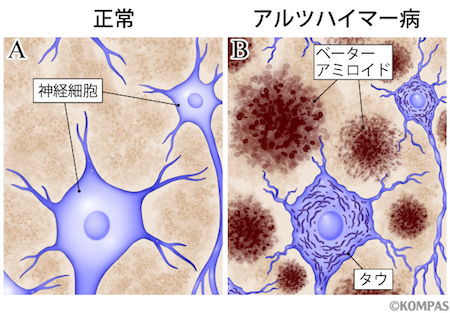
今回話題になっているアデュカヌマブは、脳内アミロイドβを減少させる、今までになかった唯一のADの根本治療を目的とした薬でした。
ADの治療薬に対する期待は大きく、米バイオジェン、日本のエーザイ共に承認申請の発表後は同社の株価は急騰し、両社の株価は1か月足らずで2倍になりました。
しかし正式承認とならなかったことや公的保険適用にならないことから次第に人気低迷し、現在株価は発表前の水準に戻っています。
現在日本で承認されているAD薬にはどのようなものがあるか?
現在発売されているアルツハイマー型認知症薬は下記の4種類があります。
①アリセプト(一般名:ドネペジル)
②レミニール(同:ガランタミン)
③メマリー(同:メマンチン)
④リバスタッチ/イクセロンパッチ(アリセプト・レミニールと同じ作用の貼り薬)
①②は脳内の神経伝達物質であるアセチルコリンを増やす目的の抗コリンエステラーゼ薬、③は同じく脳内の神経伝達物質であるグルタミン酸の異常放出を抑える目的のグルタミン酸受容体阻害薬で、この2つは薬の効き方が違うので併用できますが、いずれも根本治療のための薬ではなく「疾患の再発率の抑制や進行を遅らせる作用を持つ薬」となっています。
日本の多くの臨床医師が使っている薬の手引書「今日の治療薬(南江堂)」の、現在日本で発売されている抗認知症薬の解説ページには「服薬指導のポイント:抗認知症薬による治療の目的は症状の進行遅延である。症状が変わらないことが効いている事である点を説明する」と記載してあります。
実際、フランスでは2018年8月から、日本で承認されている4種類のAD薬すべてが副作用の割に効果が低く、薬の有効性が不十分だとして医療保険の適用対象から除外されています。
日本ではAD薬としてアリセプトが有名だが、その効果は?
アリセプトは日本のエーザイが開発し、1999年10月に認知症治療薬の承認を受け発売開始されました。そして2011年に先発医薬品の特許期間が終了し、2011年11月から後発品の発売が可能となり、現在はその後発品にシュアを奪われている状況です。
アリセプトの研究開発が始まった1983年当時は、ADの原因は神経伝達物質である脳内アセチルコリンが減少するという「アセチルコリン仮説」が主流でした。しかし、認知症以外で亡くなった方でも脳内アセチルコリンが減少していることが判り、1990年代にはアセチルコリン仮説は主流ではなくなっていました。アリセプトが販売された1990年代後半にはこのアセチルコリン仮説は既に過去のものであったとされています。
しかしAD治療薬は患者家族や社会から切望されており、進行を遅らせる効果があるのであれば承認すると言う事であったようです。
その後電子顕微鏡の進歩などでAD患者の脳内に異常に多い「老人斑」はアミロイドβであること、神経原線維変化の主成分はタウ蛋白であることが判明し、現在のAD治療薬開発の主流はこの「アミロイド仮説」を基にしたものとなっています。
アデュカヌマブなぜ承認ならなかったか
今回のアデュカヌマブは臨床試験でアミロイドβと言われる脳内の老人斑を減らす効果がある事は認められましたが、認知症の症状を減らす効果は限定的であったとの評価です。
アミロイドβが減ってもなぜ認知症症状の改善につながらなかったかについては、アミロイドβはADの「原因」ではなく、むしろ「結果」であり、ADを発症した後に薬でアミロイドβを減らしても症状を改善させることは難しいとされています。
脳内ではADの症状の出る20∼30年前からアミロイドβがたまり始め、数十年にわたり脳にダメージを与えた結果、認知症を発症した時点では既に脳内神経細胞の多くが失われた状態だと言われています。
今後は既にADを発症した方だけではなく、脳にアミロイドβがたまり始めているものの認知機能は無症状の時期(プレクリニカル期という)の方を対象に臨床試験することが考えられています。
今後の展望
今回のアデュカヌマブについては、バイオジェンが開発を中止したわけではなく、今後も投与濃度を変えるなどして治験を継続していくとしています。しかし正式承認されるかは不透明です。
そして、アデュカヌマブに続く認知症薬として、現在はイーライリリー社のドナネマブ、バイオジェンとエーザイがアデュカヌマブとは別に開発しているレカネマブ、ロシュ社のガンテネルマブなどの開発が進められていると報じられています。
いずれにせよ、新しい認知症薬が開発、製品化されるまでには10年単位の時間を要しており、現在開発中の認知症薬が製品化なるのは4~5年先であろうと言われています。

“話題|認知症の薬” に対して1件のコメントがあります。
コメントは受け付けていません。